近年来,由于矿泉水多采自无污染的地下水,并且富含各种人体所需矿 物质,而逐渐成为人们生活中的主流饮品之一。而碘离子作为人体所必需的 重要微量元素之一,在人体内具有促进和协调生物氧化、调节蛋白质合成和 分解、促进人体代谢和生长发育等重要生理作用,因而矿泉水中碘离子常被 重点关注。《GB/T 8537-2008饮用天然矿泉水》规定饮用天然矿泉水指标中 有一项为碘化物含量大于等于0.2 mg/L[1]。
碘离子的常见检测方法主要有比色法,气相色谱法,电感耦合等离子体发射光谱法以及近年来兴起的离子色谱法。比色法比较经典,但是由于使用 高毒的亚砷suan等试剂而易导致安全问题。气相色谱法需经衍生步骤,且常采 用填充柱进行色谱分离,柱效低,分离效果不理想。发射光谱法也可用于水 中碘检测,且可同时检测多种物质,但碘的检测灵敏度较低。离子色谱在碘 离子的测定上体现出比较明显的优势,且由于安培检测具有极高的灵敏度而 逐渐成为主导[2-3]。本文则着重研究了新型强亲水碳酸盐体系色谱柱结合更为 常见的抑制型电导检测技术用于碘离子测定,并成功应用于矿泉水中碘离子 含量的准确测定。
测试条件
仪器:戴安ICS-1100型离子色谱仪; 色谱柱:IonPac AS 22,6.5 µm,4 mm×250 mm (P/N: 064141); IonPac AG22,11 µm,4 mm×50 mm (P/N: 064139); 柱温:30 ℃; 流速:1.30 mL/min;
进样方式:自动进样;
定量环:500 µL; 淋洗液:4.8 mmol/L Na2CO3+1.0 mmol/L NaHCO3溶 液,等度淋洗;
检测方式:抑制型电导,离子自动电解连续再生微 膜抑制器ASRS 300,4 mm(P/N: 064554),自循环模 式,抑制电流35 mA。
样品前处理
样品通过0.22 µm尼龙滤膜过滤后,可直接进样测定。
结果和讨论
色谱柱的选择
碘离子属于典型的强极性型阴离子,常规烷基或烷 醇基季铵盐的亲水性较弱,典型色谱柱如IonPac AS14、 IonPac AS 14A和IonPac AS15,碘离子在这类色谱柱上 保留极强,往往需要借助于有机溶剂的冲洗才能缩短分 离时间和改善色谱峰形。随着色谱柱技术发展,烷醇基 季铵盐色谱柱的亲水性得到很大提高,先后出现了IonPac AS16、IonPac AS20等强亲水性色谱柱,数分钟内可完成 碘离子洗脱,峰形尖锐对称。碳酸盐淋洗液相比氢氧化钠 淋洗液具有更好的稳定性,IonPac AS22则是烷基季铵盐 和烷醇基季铵盐混合填料的碳酸盐体系色谱柱,使得该碳 酸盐体系色谱柱的亲水性得到很大改善。经实验证明,碘 离子在AS22上可以在15分钟内被洗脱,见图1,而无需 借助有机溶剂分离强极性阴离子。
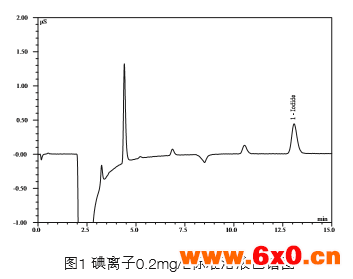
标准曲线和方法检出限
碘离子在0.01-10 mg/L浓度范围内都具有良好的 线性,标准曲线拟合方程见表1所示,相关系数分别为 0.9998。根据3倍信噪比(Signal/Noise=3)可分别计算 出碘离子的检出限为4 µg/L。
方法重现性、回收率及样品测试结果
将样品经过滤后直接进样分析,图2为某碘泉矿泉 水样品及加标谱图对比。表2为部分样品的测定数据(3 个阴性样品和3个阳性样品),阳性样品的三次平行处 理进样测得碘离子的相对标准偏差均在3%以下。分别 对这六个样品分别进行加标回收实验,加标回收率在 96.8~102.4%之间,表明矿泉水中所含有的高浓度盐分 对碘离子测定不存在明显影响。本方法用于实际矿泉水 样品中碘离子可以得到良好的重现性和较高的准确性, 以此方法测定了市场上采集的矿泉水样12种,经检测后 存在碘离子的样品共有3组,其中仅有一组含有高于0.2 mg/L以上的碘离子
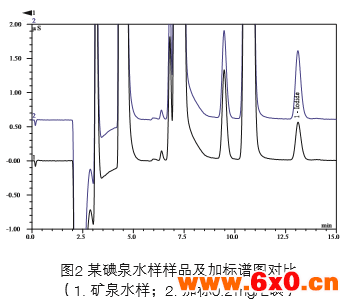
结论
建立了一套快速测定矿泉水中碘离子的抑制型电导 离子色谱方法,利用碳酸盐体系亲水性阴离子交换色谱 柱IonPac AS22进行分离,样品中的碘离子可以在15 min 内被完全洗脱,而矿泉水中含有的大量氯离子、硫酸根 等不影响碘离子的分析。该方法所需离子色谱仪配置较 低,淋洗液的配制方法简单,结果稳定可靠,更容易在 检测领域内得到推广。










 QQ交流群
QQ交流群

